KNOWLEDGE
首頁
教師資源
KNOWLEDGE
首頁
教師資源
化學科課程-溶解度
![]() MAR 04 ,2019
MAR 04 ,2019
<翻譯自PASCO智慧圖書館,轉載請註明出處>
簡介
大多數的物質皆可以溶解在水中,然而不同物質溶解的程度與溶解後表現的形式不會相同。分子化合物(Molecular compound)以分子(Molecular)的狀態表現於水中,離子化合物(Ionic compound)則以離子(Ion)的狀態表現,也因此對水溶液產生了導電性。難溶性的物質仍會溶解些微的物質,若這些物質為重金屬離子(例如鉛、鉈、鎘),極少量就有可能對人體造成影響,所以了解物質在水中的溶解程度,可以幫助了解更多的潛在危險因子。
實驗前動動腦
- 為什麼當加入溶質後,溶液的導電度發生改變?
- 根據偵測導電度,要如何區分溶解的物質為離子化合物或分子化合物?
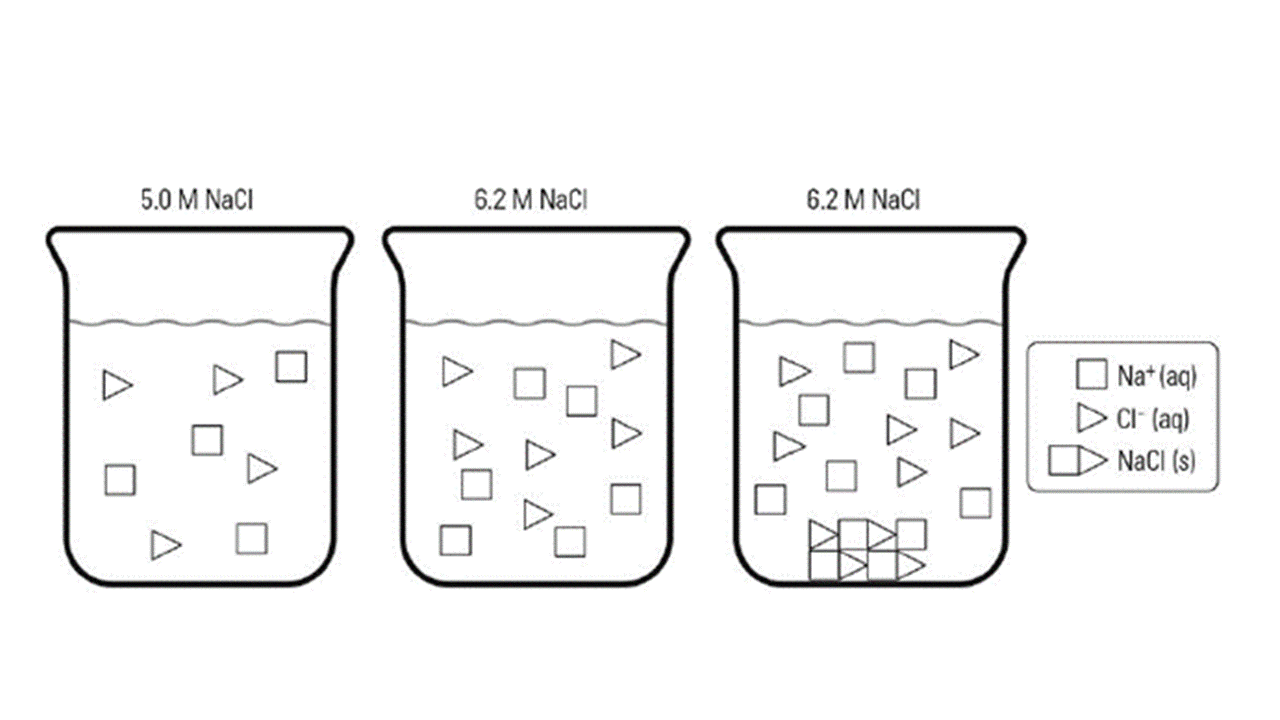
- 下圖為3瓶燒杯,何者屬於飽和溶液?何者屬於未飽和溶液?
4. 酒石酸(KHC4H4O6)之後的解離方程式可寫成: KHC4H4O6(s) ⇌ K+(aq) + HC4H4O6–(aq),試描述在飽和水溶液的狀態下的正反應與逆反應
實驗搭配設備

 Facebook
Facebook

 LINE
LINE